Уважаеми Медицински специалисти,
Bayer AG в съгласие с Европейската агенция по лекарствата (ЕМА) и Изпълнителната агенция по лекарствата (ИАЛ) бихме искали да Ви информираме за следното:
Резюме
- Случаи на повишено вътреочно налягане са съобщавани по-често (изчислено приблизително като седем-кратно увеличение на съобщаване) при използване на Eylea предварително напълнена спринцовка в сравнение с използване на Луер-лок спринцовката на Eylea инжекционен разтвор във флакон.
- Подозира се, че неправилно боравене по време на подготовка и инжектиране са най-вероятната първопричина за наблюдаваните случаи на повишено вътреочно налягане с Eylea предварително напълнена спринцовка. Инжектирането трябва да се извършва от медицински специалисти с опит в приложението на тази лекарствена форма.
- Правилното боравене с предварително напълнената спринцовка и обучението са ключови за намаляване на този риск:
- използвайте 30 G х 12 mm инжекционна игла.
- винаги проверявайте дали излишният обем/въздушните мехурчета в предварително напълнената спринцовка са отстранени преди употреба: основата на свода на буталото (не върха на свода на буталото) трябва да бъде изравнена с черната линия за дозиране на спринцовката (вижте по-долу);
- внимателно натискайте буталото;
- прилагайте точно препоръчителната доза и не инжектирайте никакъв остатъчен обем, тъй като повишеният инжекционен обем може да доведе до клинично значимо повишение на вътреочното налягане.
- Оценявайте зрението на пациента и проследявайте вътреочното налягане непосредствено след интравитреалната инжекция.
Обща информация
Eylea предварително напълнена спринцовка e показан при възрастни за лечение на:
- неоваскуларна (влажна) възрастовообусловена дегенерация на макулата (ВДМ)
- зрително увреждане, дължащо се на оток на макулата, вследствие на оклузия на ретинална вена (ОРВ) (оклузия на разклонение на ретинална вена (ОРРВ) или оклузия на централната ретинална вена (ОЦРВ))
- зрително увреждане, дължащо се на диабетен макулен едем (ДМЕ)
- зрително увреждане, дължащо се на миопична хороидална неоваскуларизация (миопична ХНВ)
Повишаване на вътреочното налягане е известна нежелана лекарствена реакция, свързана с интравитреалните инжекции като цяло, включително и с употребата на Eylea. Седемкратно увеличение на честотата на съобщаване на повишено вътреочно налягане е било съобщено с предварително напълнената спринцовка (приблизително 1,1 случая на 10 000 продадени предварително напълнени спринцовки спрямо 0,15 случая на 10 000 продадени флакона), считано от скорошното пускане на пазара в Европа на този продукт през месец април 2020 г. Има съобщения за преходно повишаване на вътреочното налягане и обратимо зрително увреждане след интравитреални инжекции. При мнозинството от случаите с известен изход е настъпило възстановяване без трайни последици.
Не са установени дефекти в качеството на Eylea предварително напълнените спринцовки или на инжектирания разтвор. След по-задълбочен преглед на докладваните случаи, се подозира, че причината за повишеното вътреочно налягане е приложението и на излишния остатъчен обем от продукта, вследствие на неправилно боравене по време на подготовката и инжектирането. Освен това, Eylea предварително напълнена спринцовка е стъклена спринцовка с гумено бутало, което изисква използването на малко повече сила в сравнение с пластмасовите спринцовки (като тези, използвани с флакона).
За допълнително намаляване на риска, трябва стриктно да се следват следващите препоръки за правилно боравене с Eylea предварително напълнена спринцовка:
- Трябва да се използва 30 gauge х 12 mm инжекционна игла.
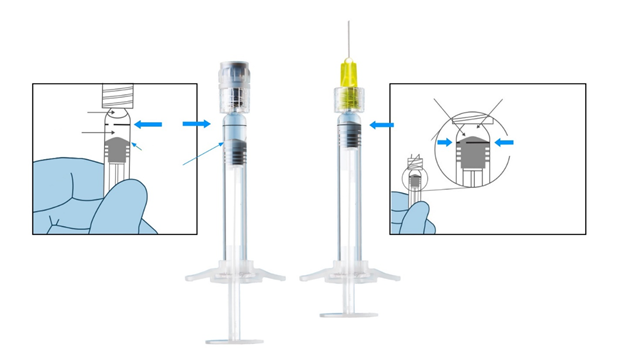
- За да отстраните всички мехурчета и да изтласкате излишния лекарствен продукт, буталото трябва да бъде правилно позиционирано. Основата на свода на буталото (не върха на свода на буталото) трябва да е изравнена с черната линия за дозиране на спринцовката, както е описано в секция „Указания за употреба на предварително напълнената спринцовка:“ от продуктовата информация и на фигурата по-долу.
- При приложение на дозата в окото, буталото трябва да се натиска внимателно с непроменлив натиск, докато буталото достигне дъното на спринцовката. Малък остатъчен обем от разтвора може да се наблюдава в спринцовката след като буталото е достигнало дъното на спринцовката. Не се опитвайте да го приложите като упражнявате допълнителен натиск върху буталото.
Вътреочното налягане трябва да се проследи и ако е необходимо, трябва да се започне подходящо лечение. Непосредствено след интравитреалната инжекция:
- Оценете зрението (движение на ръка или броене на пръсти).
- Подходящото проследяване може да включва проверяване на перфузията на диска на зрителния нерв или тонометрия. Трябва да има на разположение стерилно оборудване за парацентеза.
Препоръчително е да се прави справка с предоставените обучителни материали и разпространената информация относно правилната употреба на предварително напълнената спринцовка, представена в Ръководството за предписващия лекар и видеото относно инжектирането от обучителните материали за Eylea. Обучителните материали, включително и Ръководство за пациента, могат да бъдат намерени също и на https://www.edumaterial.bayer.bg или могат да бъдат предоставени допълнително при поискване, заедно с обучителни сесии.
Продуктовата информация и обучителните материали за медицинските специалисти се актуализират, за да съдържат допълнителни инструкции/препоръки относно боравенето с предварително напълнената спринцовка, за да се намали риска от повишаване на вътреочното налягане.
Призив за съобщаване на нежелани лекарствени реакции
Бихме искали да напомним, че медицинските специалисти са задължени според Закона за лекарствените продукти в хуманната медицина (ЗЛПХМ) да съобщават незабавно на притежателя на разрешението за употреба или на Изпълнителна агенция по лекарствата (ИАЛ) за всяка подозирана сериозна нежелана лекарствена реакция и да предоставят при поискване допълнителна информация от проследяването на случая.
Изпълнителна агенция по лекарствата (ИАЛ)
ул. „Дамян Груев“ №8
1303, гр. София
Р. България
Тел: +359 2 8903 417
Факс: +359 2 8903 434
e-mail: Този имейл адрес е защитен от спам ботове. Трябва да имате пусната JavaScript поддръжка, за да го видите.
Формуляр за съобщаване на нежелани лекарствени реакции от медицински специалисти
Съобщавайте нежеланите реакции на Изпълнителна агенция по лекарствата:
- тел.: +359 2 8903417
- e-mail: Този имейл адрес е защитен от спам ботове. Трябва да имате пусната JavaScript поддръжка, за да го видите.
Онлайн:
 Формуляр за съобщаване на нежелани лекарствени реакции от медицински специалисти
Формуляр за съобщаване на нежелани лекарствени реакции от медицински специалисти
Притежател на разрешението за употреба
Байер България ЕООД
Диана Илиева - Ръководител Лекарствена безопасност
ул. „Резбарска“ 5, София 1510
тел.: +359 2 81 401 02
мобилен: +359 887 77 00 24
факс: +359 2 81 401 09


